| Climat & Transferts thermiques |
Ramenée à la
pression atmosphérique, la couche d'ozone
représenterait 3 mm
Qu'en serait-il pour les autres gaz ?
Données : voir page
précédente.
Par mole, l'air pèse : 76% de N2 + 23% O2 + 1% Ar = 0,76*28 + 0,23*32 + 0,01*80 = 29 g/mol
Ainsi, une "mole d'air" pèse 29 grammes (un peu plus qu'une mole de N2).
A 0,029 kg/mole, 10,1 Tonnes sont constituées de 348276 moles. A T=15°C et P=1 atm, selon la loi des gaz parfaits : V= (348276x8,32x288/101300=) 8238 m3, c'est à dire une hauteur de 8 km environ pour 1 m2 de surface.
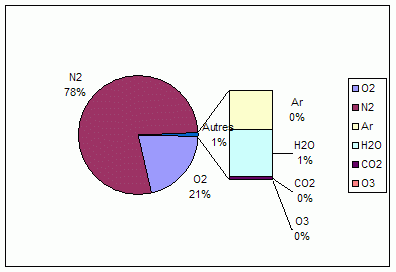 |
* Pour l'azote, la hauteur serait
de
(3877Tt//510M.km²/28x8,32x288/101300=) 6,422 km
.
* Pour
l'oxygène, la hauteur serait de
(1188Tt/510M.km²/32x8,32x288/101300=) 1,722
km
.
* Pour l'argon, la hauteur serait de
(66Tt/510M.km²/80x8,32x288/101300=) 38 m
.
* Pour
la vapeur d'eau, la hauteur serait de
(17Tt/510M.km²/18x8,32x288/101300=) 44
m
.
* Pour
le gaz carbonique, la hauteur serait de
(2,5Tt/510M.km²/46x8,32x288/101300=) 3
m
|